Vertex Pharmaceuticals
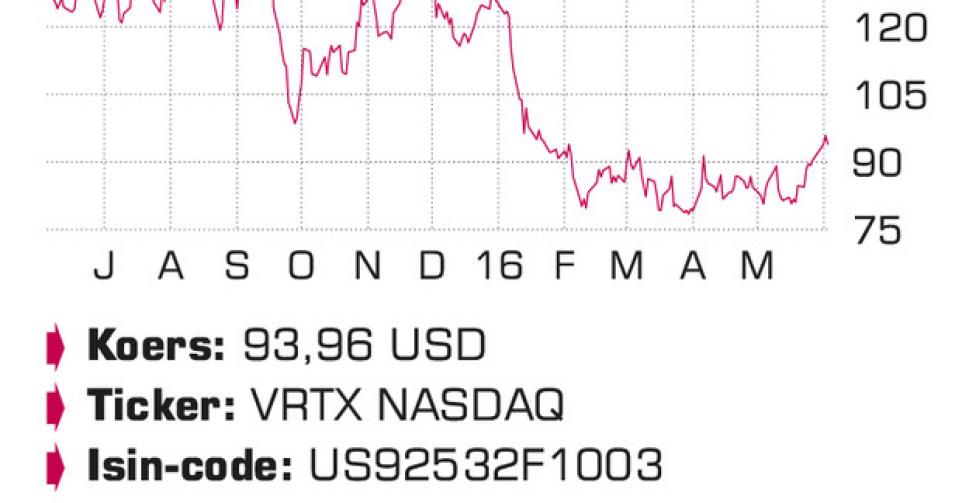
Ondanks de minder sterke groeicijfers van Orkambi en de opkomende concurrentie blijft de leiderschapspositie van Vertex Pharmaceuticals in de behandeling van de taaislijmziekte de eerste jaren onaantastbaar.
Vertex Pharmaceuticals, de voormalige portefeuillewaarde, noteert nog altijd 25% lager dan eind 2015. De belangrijkste verklaring is de tot nu tegenvallende toename van de verkoop van Orkambi, na Kalydeco het tweede product dat onderliggende genmutaties aanpakt die verantwoordelijk zijn voor de taaislijmziekte of mucoviscidose. Orkambi is een combinatietherapie van een potentiator (Kalydeco) en een corrector (Lumacaftor, VX809) voor de behandeling van de homozygote vorm van de F508del-mutatie, een mutatie die verantwoordelijk is voor 8500 patiënten ouder dan twaalf jaar in de Verenigde Staten en 12.500 patiënten in Europa. Het product werd gelanceerd in juli 2015.
De gerealiseerde omzetcijfers in het derde en vierde kwartaal, respectievelijk 130,8 miljoen USD en 219,9 miljoen USD, waren nog meevallers, maar de bijna nulgroei in het eerste kwartaal (223 miljoen USD) ontgoochelde, omdat meer patiënten dan verwacht (15%) de behandeling binnen de drie maanden stopzetten als gevolg van nevenwerkingen. Vertex gaf daarop ontgoochelende jaarverwachtingen voor Orkambi: 1 à 1,1 miljard USD omzet, tegenover een consensus van 1,3 miljard USD (eind 2015 zelfs nog 1,6 miljard USD). Het feit dat eind maart – slechts negen maanden na de goedkeuring – 65% van de doelgroep (5500 patiënten op een totaal van 8500) een behandeling had opgestart, blijft evenwel een sterk cijfer, en Vertex mikt tegen eind 2016 op 90%. De bijdrage vanuit Europa (9 miljoen USD omzet in het eerste kwartaal) is voorlopig nog beperkt tot Duitsland, maar vanaf 2017 zal de omzet er sterk toenemen.
De verwachte piekverkoop voor Orkambi bedraagt nog steeds minstens 4 miljard USD. Positief is alvast dat de FDA, het Amerikaanse geneesmiddelenagentschap, een aanvraag tot versnelde goedkeuring aanvaardde voor het gebruik bij patiënten tussen zes en elf jaar (doelgroep van 2500 patiënten), met voorziene beslissing in het vierde kwartaal. De omzet van Kalydeco (doelgroep van 4000 patiënten) bedroeg in het eerste kwartaal 171 miljoen USD, +31% tegenover het eerste kwartaal in 2015, maar wel -5,5% tegenover het vorige kwartaal. De verwachte jaaromzet werd verhoogd, van 670 à 690 miljoen USD naar 685 à 705 miljoen USD. Vertex koestert nog steeds de steile ambitie om op termijn in taaislijmziekte minstens 90% van de totale doelgroep van 75.000 patiënten in Noord-Amerika, Europa en Australië te bereiken.
Dat vereist wel een doorbraak voor de moeilijkst te behandelen patiënten, die met de heterozygote F508del-mutatie (17.000 patiënten). Vanaf de tweede jaarhelft starten hiervoor met correctors VX-152 en VX-440 meerdere triple-combinatietherapieën, met potentiator Kalydeco en corrector VX661. Vertex onderzoekt ook mogelijkheden voor betere werkzaamheid bij bestaande doelgroepen. De eerste resultaten worden begin 2017 verwacht, met mogelijke marktlancering in 2018. Vertex behoudt nog steeds een jaar voorsprong op de concurrerende onderzoeken van Galapagos met partner AbbVie.
Conclusie
Ondanks de wat minder sterke groeicijfers van Orkambi en de opkomende concurrentie blijft de leiderschapspositie van Vertex Pharmaceuticals in taaislijmziekte de eerste jaren onaantastbaar. Het aandeel blijft echter duur, tegen 20 keer de verwachte winst 2017.
Advies: houden/afwachten
Risico: gemiddeld
Rating: 2B
Aandelen België
Fout opgemerkt of meer nieuws? Meld het hier